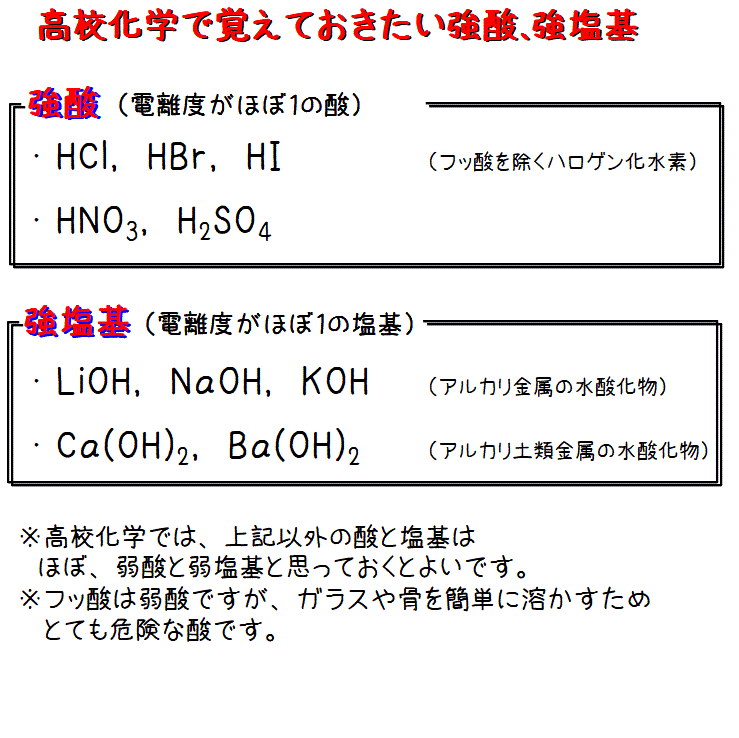
酸と塩基は、電離度の違いで強酸・強塩基(電離度≒1)と弱酸・弱塩基(電離度<<1)にわけられますが、弱酸、弱塩基は限りなくありますので、高校化学の場合は、乱暴な覚え方かもしれませんが、例に挙げた強酸と強塩基以外は、弱酸と弱塩基と思っておくと良いです。
基本的には
・強酸は、硫酸、硝酸とフッ酸を除くハロゲン化水素
・強塩基は、アルカリ金属とアルカリ土類金属の水酸化物
です。
(余談ですが、フッ酸は弱酸ですが、ガラスや骨を溶かすので、とても危険な酸です。そしてフッ酸は半導体製造には欠かせない薬品です。
私が半導体メーカーでエンジニアをしていた時は、実験でよくフッ酸を使っていましたが、ドラフトチャンバー内で手袋を二重にして扱い、また蒸気を吸ったら歯が溶けると言われていて、定期的に歯科検診も受けさせられてました。)
なぜ、強酸、弱酸、強塩基、弱塩基を区別して覚えとかないといけないかというと、中和してできた塩の水溶液が何性を示すか、遊離反応をするのかしないのかなどの判断に使えるからです。
必ず覚えておきましょう。
